“Una minaccia apocalittica”. Così Dame Sally Davies, consulente del Ministero della Salute britannico, ha definito il problema della resistenza dei batteri agli antibiotici in un discorso al Parlamento. Un problema, questo, sempre più diffuso negli ospedali di tutto il mondo causato dall’uso eccessivo di antibiotici e aggravato dalla capacità dei batteri di trasmettersi l’un l’altro i geni che li rendono insensibili ai farmaci usati. Di fronte ad un nemico così adattabile cosa si può fare? Una strategia potrebbe essere quella di impedire ai batteri di scambiarsi i geni con cui si difendono dagli antibiotici. In quest’ottica, uno studio pubblicato su Pnas da un gruppo di ricercatori americani ha identificato il meccanismo molecolare tramite cui la resistenza agli antibiotici viene passata da un batterio all’altro e ha dimostrato che bloccando questa via si può ridurre la capacità dei batteri di diventare resistenti ai farmaci.
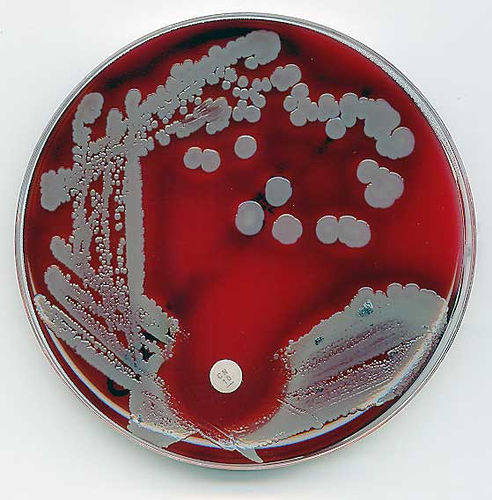
Per i loro esperimenti gli scienziati dell’Università della North Carolina hanno usato alcuni ceppi di Staphylococcus aureus, resistenti all’antibiotico vancomicina, detti anche Vrsa (vancomycin-resistent S. aureus). Lo S. aureus è un comune batterio presente sulla cute, che può causare infezioni negli esseri umani, curate in genere con antibiotici quali le penicilline. Fanno parte di questa famiglia anche i famigerati Mrsa (S. aureus meticillino-resistente) divenuti una delle principali cause delle infezioni ospedaliere, finora trattate efficacemente solo con la vancomicina.
“Ci siamo concentrati sui Vrsa per cercare di capire come viene acquisita la resistenza alla vancomicina”, spiega Jonathan Edwards, primo autore dello studio: “perché in questo ceppo è stato isolato il primo elemento genetico che conferisce resistenza a questo antibiotico”. Si tratta di un frammento di Dna circolare, il plasmide pLW1043, che durante il processo di coniugazione – in cui due batteri vengono in contatto e si scambiano materiale genetico – viene trasferito da un microrganismo all’altro. Il plasmide pLW1043 contiene i geni necessari per la sopravvivenza in presenza di antibiotico e richiede l’azione di una proteina per potersi trasferire da un batterio all’altro: la Nes o nicking enzyme, che permette il processo di mobilizzazione, tagliando il Dna plasmidico nel batterio donatore e rilegandolo in quello ricevente a trasferimento avvenuto.
Usando dati di cristallografia e diffrazione ai raggi X, che permettono di determinare la struttura tridimensionale di una proteina, i ricercatori hanno identificato due regioni chiave per il funzionamento dell’enzima, che formano una zona in cui il plasmide contenente i geni per la resistenza viene modificato per essere trasferito. Se la struttura di questa regione cambia, o se ne impedisce il legame con il Dna, si blocca il trasferimento del plasmide da un batterio all’altro. Infatti, sulla base della struttura cristallina della Nes, gli scienziati hanno disegnato un polimero sintetico di poliamine in grado di legarsi specificamente al Dna plasmidico impedendo l’azione della Nes e hanno osservato una riduzione di circa il 90% dell’attività enzimatica.
“Questo risultato è davvero promettente – afferma Edwards – perché potrebbe portare in futuro allo sviluppo di nuovi metodi per bloccare la propagazione della resistenza agli antibiotici inibendo il trasferimento dei geni di resistenza da un batterio all’altro”.
Secondo gli esperti il problema della resistenza agli antibiotici è uno dei maggiori rischi per la salute umana, una vera e propria emergenza sanitaria globale. Le infezioni che non rispondono più ai trattamenti antibiotici finora usati, come la tubercolosi, la Mrsa e la gonorrea, sono in continuo aumento. E diventa sempre più lungo e costoso produrre nuovi antibiotici. Pertanto, secondo l’Oms, finché la ricerca non riuscirà a trovare una soluzione migliore, le uniche possibilità per arginare la diffusione dell’antibiotico-resistenza sono migliori condizioni igieniche e un uso più consapevole degli antibiotici.
Riferimenti: Pnas Doi:10.1073/pnas.1219701110
Credits immagine: estherase/Flickr