I fermenti lattici – quei batteri benefici capaci di trasformare il latte in yogurt e i cavoli in crauti –sono considerati un toccasana per la salute, tanto da averli battezzati come “probiotici”. Ma perché? Come agiscono nel nostro intestino e in che modo rafforzano il sistema immunitario? Per rispondere a questa domanda, ancora insoluta, uno studio dell’Università di Lipsia – pubblicato su Plos Genetics– ha indagato la stretta relazione tra i lattobatteri contenuti in molti cibi fermentati (yogurt, kefir, crauti, té nero) e un recettore presente sulle cellule di esseri umani e grandi scimmie. Scoprendo così che è capace di accelerare gli effetti benefici dei fermenti lattici sul sistema immunitario e i processi antinfiammatori. E che probabilmente si tratta di un “regalo” dell’evoluzione, eredità di un nostro lontano antenato che per primo poté apprezzare i cibi non proprio freschi, come un fico caduto dall’albero e già in fermentazione.
Perché i lattobacilli aiutano il sistema immunitario?
I fermenti lattici o LAB comprendono una varietà di batteri Lactobacillus (acidophilus, casei, Delbrueckii e altri) che hanno proprietà benefiche sull’organismo poiché producono una sostanza (metabolita) chiamata D-PLA che ha proprietà antimicrobiche che aiutano il buon funzionamento del sistema immunitario. La cosa è assodata, tuttavia, ancora non è ancora del tutto chiaro in che modo questi LAB intervengano sulla fisiologia umana e per quale motivo siano entrati maggiormente nell’alimentazione di alcuni mammiferi invece che di altri. Per capirne di più, i ricercatori tedeschi hanno pensato quindi di studiare il rapporto tra fermenti lattici e alcuni recettori degli acidi idrossicarbossilici (HCAR) che regolano le funzioni immunitarie.
Una chiave speciale per i fermenti lattici
In quasi tutti gli animali, infatti, sono presenti due tipi di recettori degli acidi idrossicarbossilici (HCAR), chiamati HCA1 e HCA2. Esseri umani, gorilla e scimpanzé ne hanno però uno in più: HCA3. Ed è proprio su questo particolare recettore che il gruppo di Claudia Stäubert ha condotto uno studio in vitro e in vivo per capire che tipo di interazione ha con i fermenti lattici e in che modo la sua presenza possa essere stata vantaggiosa nell’evoluzione umana. Con tecniche avanzate come la cromatografia liquida-spettroscopia di massa (LC-MS), lo studio ha dimostrato che, quando mangiamo cibi fermentati, il D-PLA viene assorbito molto velocemente dall’organismo, raggiungendo un’alta concentrazione nel sangue che attiva i recettori HCAR.
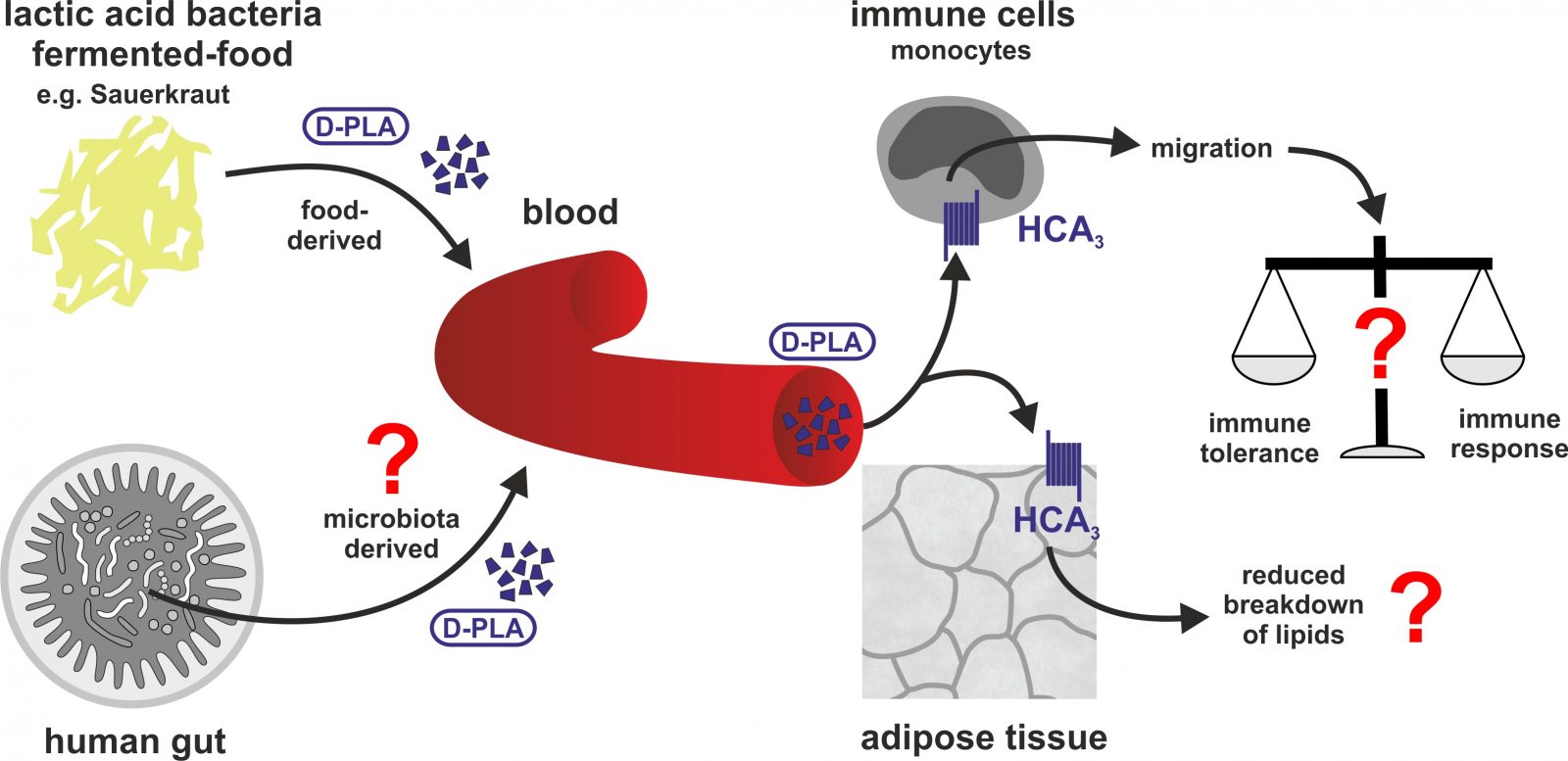
In altre parole: i metaboliti, legandosi fortemente ai recettori, “segnalano” al sistema immunitario la loro presenza innescando una serie di reazioni benefiche, per esempio, nei processi di tipo antinfiammatorio. Effetti benefici che ulteriori studi potranno chiarire nel dettaglio.
HCA3, una marcia in più per la sopravvivenza
Ma la vera scoperta è che la forte selettività dei D-PLA verso i recettori HCA3 rispetto a quella mostrata nei confronti degli altri due recettori HCA rende tutto il processo molto più rapido. Per nostra fortuna, siamo tra i pochissimi mammiferi a possedere questa variante del recettore HCA. Ma come ci siamo trovati ad entrare in un club così esclusivo, che comprende solo noi e le altre grandi scimmie?
Incrociando dati di laboratorio con dati archeologici, i ricercatori hanno scoperto che abbiamo ereditato questo recettore speciale da un antenato in comune con gorilla e scimpanzé. Un antico primate che, grazie a questa “innovazione”, poté iniziare a nutrirsi anche della frutta caduta dagli alberi e già in fermentazione a causa dei naturali processi di decomposizione. Un bel vantaggio per la sopravvivenza.
Dall’evoluzione alle cure future
Lo studio offre quindi nuove informazioni sulle dinamiche co-evolutive che interessano i microbi e i loro ospiti umani, sui molteplici effetti positivi del consumo di cibi fermentati e sull’evoluzione della nostra specie. Ma apre anche nuove strade per lo sviluppo di nuovi farmaci e terapie, che sfruttino il recettore HCA3 percontrastare le malattie legate al sistema immunitario. “Siamo convinti che questo recettore sia mediatore di alcuni effetti benefici e anti-infiammatori garantiti dai fermenti lattici– spiega la coordinatrice dello studio Claudia Stäubert – e pensiamo quindi che potrebbe servire come potenziale bersaglio di farmaci per il trattamento di malattie infiammatorie”.
Riferimenti: Plos Genetics






