La chimica intesa come scienza sperimentale si sviluppa nel XVII secolo, in un processo che vede collaborazioni e contrapposizioni tra le idee e le teorie di studiosi inglesi, francesi, italiani e russi. In questo periodo infatti si cominciarono a sviluppare ipotesi ed esperimenti su diversi modelli di struttura della materia e sui processi di trasformazione delle sostanze. I nomi di Dalton, Proust, Lavoisier, Gay-Lussac, Avogadro e Mendeleev sono ben noti agli studenti di liceo, che ricordano leggi e tavole col loro nome, forse senza averne afferrato a pieno l’originalità e il significato concettuale. Tanto più che, come racconta lo storico della scienza Marco Ciardi, il racconto rituale dei manuali scolastici non sempre coincide con quello che effettivamente proposero gli scienziati nella loro epoca e certamente non rispecchia la tensione concettuale delle loro interpretazioni. E’ quindi particolarmente interessante seguire il percorso proposto da Ciardi, perché permette di connettere logicamente e non solo storicamente lo sviluppo del pensiero chimico fino alla sistematizzazione data da Mendeleev alla serie degli elementi.
L’origine degli elementi
Ovviamente si comincia da lontano, ricordando come Democrito, ai suoi tempi, avesse immaginato una materia divisibile, composta da elementi indivisibili da lui chiamati atomi. Ma ancora verso la metà del ’700 si conoscevano soltanto alcune delle sostanze che chiamiamo elementi e ad altre, definite con i criteri e la terminologia alchemica, si attribuivano proprietà e composizione piuttosto fantasiose.
La strumentazione disponibile era ingegnosa e precisa: si facevano misure accurate di pesi e volumi di sostanze gassose… di cui però non si identificava la struttura. Le “piccole parti” che formavano la materia venivano chiamate corpuscoli, particole, particelle, molecole, atomi. C’erano corpuscoli primari e corpuscoli derivati, i chimici francesi chiamavano molecole quello che gli inglesi chiamavano atomi, gli atomi potevano essere semplici o complessi e le molecole potevano essere costituenti (o elementari: gli atomi di oggi) o integranti (o complesse, o integrali).
Le tavole di affinità
L’esperienza permetteva di costruire Tavole di affinità tra le diverse sostanze e si immaginavano forze di attrazione o repulsione che governavano la formazione di composti farmaceutici, adatti per varie terapie. Per tentare di risolvere la confusione tra i nomi delle sostanze, e considerando metodologicamente più efficace l’approccio quantitativo rispetto all’approccio qualitativo, ai tempi della Rivoluzione Francese, Lavoisier aveva proposto un “Metodo di nomenclatura chimica”, un “Trattato elementare di chimica”, e aveva anche definito una legge di conservazione della materia trovando che la massa dei prodotti di una reazione è sempre uguale alla massa delle sostanze reagenti. Purtroppo Lavoisier non poté concludere il suo lavoro da chimico perché venne ghigliottinato durante il Terrore, nel 1794.
L’evoluzione del pensiero chimico
In questo quadro dinamico, stimolante e confuso Ciardi comincia a mettere in evidenza le grandi linee di pensiero su cui si è fondata la scienza chimica, illustra i contrasti tra Berthollet e Dalton sulla “legge delle proporzioni definite” secondo cui potevano combinarsi le diverse sostanze, racconta la vera storia della ipotesi di Avogadro sulla struttura chimica dell’acqua, diversa da quella raccontata sui manuali scolastici. Siamo ormai nel 1841 e, nella sua opera chiamata “Fisica dei corpi ponderabili” Avogadro sostiene che le molecole integranti dei gas (nel suo caso di O2) dovevano essere formate da un gruppo di molecole semplici (nel suo caso: due molecole elementari O+O, che oggi corrispondono ai nostri atomi).
Di questi costituenti elementari dei gas, però, Avogadro pensava che non si potesse sempre indicare il numero né considerarlo costante in tutte le sostanze gassose: i suoi risultati non erano dunque generalizzabili. Usando tecnologie diverse e molto raffinate, Ampère e Avogadro riuscirono infine a definire il numero costante di particelle presenti in volumi uguali di gas, e finalmente Cannizzaro nel luglio del 1860 al Convegno Internazionale di Karlsruhe presentò il suo “Sunto di un corso di filosofia chimica” in cui enunciò chiaramente la distinzione tra i concetti di atomo e di molecola, offrendo ai colleghi un metodo per la determinazione dei pesi atomici.
Catalogare gli elementi
Mendeleev, presente al convegno insieme al chimico-musicista Borodin, riconobbe l’importanza del contributo di Cannizzaro e lo considerò un punto di riferimento essenziale per le sue elaborazioni future. Ciardi mette bene in evidenza i vari tentativi dei chimici dell’epoca per catalogare e trovare un ordine agli elementi che via via venivano identificati, e racconta con interessanti dettagli i numerosi aggiustamenti elaborati da Mendeleev nella elaborazione della sua Tavola. Infatti nel 1898, per preparare un manuale in cui la chimica fosse strutturata come sistema unitario, Mendeleev progettò per i suoi studenti uno schema che illustrava le caratteristiche dei 63 elementi allora conosciuti.
Ordinandoli per peso atomico, cioè scegliendo una proprietà che cresce con regolarità e seguendo un criterio quantitativo, Mendeleev riuscì a non tener conto di altre proprietà degli elementi (ottiche, magnetiche,elettriche…) rimandando direttamente alla affinità naturale tra gli elementi stessi. Come risulta dalle rappresentazioni grafiche che affascinano ancora oggi, l’ordine per peso dato da Mendeleev permise di trovare periodicità anche per altre caratteristiche delle sostanze.
Intanto, la spettroscopia aveva fatto progressi ed era stato individuato un elemento simile all’alluminio che andava giusto a riempire un posto lasciato vuoto da Mendeleev nella sua tavola. Questo fatto aveva riempito di orgoglio e di commozione il chimico russo che aveva potuto constatare così l’esattezza delle sue previsioni. La sua legge generale aveva individuato una causa unitaria per la molteplicità degli elementi, indipendente dalla loro natura, e aveva aperto alla scienza un nuovo e più vasto campo di speculazione.
Il numero atomico
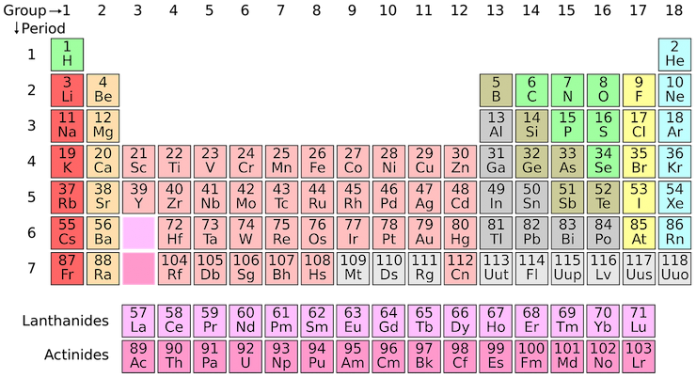
Proprio perché la scienza non può mai dire su nulla l’ultima parola lasciando sempre aperto il campo a nuove e più approfondite elaborazioni, Mendeleev era anche interessato alle proposte di migliorare la sua opera e di adeguarla alle nuove scoperte: infatti nel 1913 Moseley propose di ordinare gli elementi in base al numero atomico, così che nella Tavola moderna questo compare insieme al numero di massa accanto al simbolo dell’elemento.
Finora, conclude Ciardi, agli elementi naturali sono stati aggiunti elementi artificiali, super pesati e instabili, e la ricerca sta cercando di sintetizzare l’elemento 119, domandandosi se esista un numero definito di elementi e quale potrebbe essere l’ultimo elemento possibile. In appendice, oltre alla Tavola periodica composta da 118 elementi Ciardi riporta tre lettere inedite scritte da Mendeleev a Cannizzaro e a Piccini, altro noto scienziato italiano, per chiedere informazioni sui sistemi di pesi e misure internazionali ancora non in uso in Russia e, in previsione della fine dei suoi giorni, per salutare colleghi a cui doveva i fondamenti del suo lavoro e dire addio alla bella Italia.